《自然》技术专栏主要包含以下两种类型:
技术特写(Technology Features) | 技术新闻(Technology News) | |||
为什么选择《自然》技术特写?
技术新视野 | 内容扎实、可读性高 | 广泛的受众 | |||||
往期《自然》技术特写专题
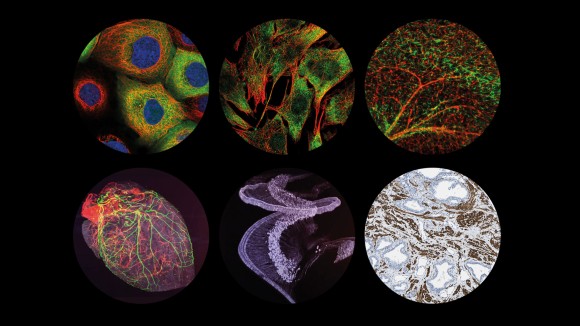 空间蛋白质组学 | 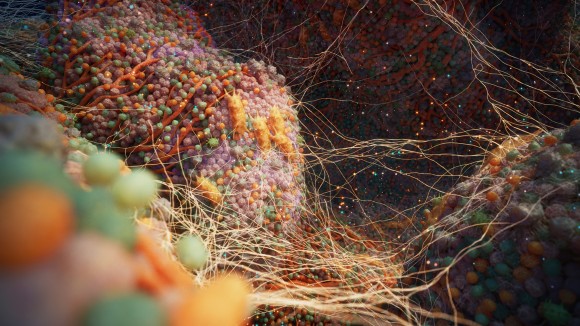 空间生物学 | 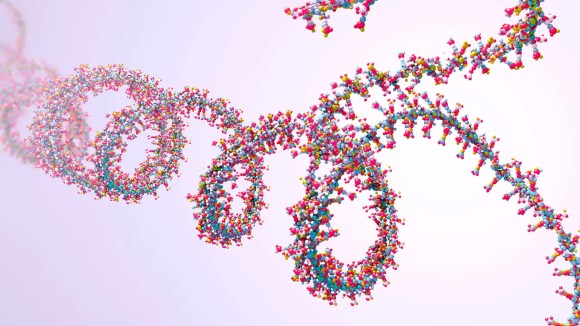 环状 RNA | |||||
4月2日 | “自驱动实验室”是一种自主实验室,在其中,人工智能与自动化结合推动研究进展而无需人为干预。本期《自然》技术特写将探访一家位于瑞典的自驱动实验室,报道它的样貌、运作方式、能力与局限,以及研究人员如何与它协作。 | ||
5月7日 | MPRAs,即“大规模平行报告基因检测”,用于同时测量大量DNA序列的基因调控活性。它们为“基因组AI”系统提供数据,使其能够“设计”出具有特定活性的全新序列(例如在特定细胞类型中发挥作用的新型调控DNA用于基因治疗)。本期《自然》技术特写将重点介绍MPRAs的应用。 | ||
5月21日 | 人工智能应用于抗生素发现主要有两种途径:利用AI从基因组序列推断某个生物体可能合成的代谢产物,进行合成和测试;利用AI直接设想全新的分子。本期《自然》技术特写将关注人工智能在抗生素诞生过程中的助力。 | ||
6月4日 | 虚拟细胞,即通过计算机、AI对细胞工作方式进行详细模拟,本质上是一系列数学模型整体描述某个或全部生化过程。本期《自然》技术特写将介绍这些模型是什么、如何运作、可能的用途及现状。 | ||
7月16日 | 本期《自然》技术特写将探讨表观基因组编辑常使用的基因组编辑系统,不是改变DNA序列,而是改变其在细胞中的化学修饰。这些修饰(如甲基化或乙酰化)会影响DNA在细胞中的读取方式,即决定基因是否表达,而不依赖于序列本身。 | ||
7月30日 | 流行的CRISPR-Cas9系统会在DNA中产生双链断裂,复杂化编辑过程。有时这些断裂会通过修复机制引入突变,而不是预期的改动。相比之下,Prime editing和碱基编辑器无需这种破坏性断裂即可改变DNA序列,它们在需要精确基因组修改的人类基因治疗等应用中尤其有前景。即便如此,这些编辑器(以及其他方法)仍有无法做到的地方。本期《自然》技术特写将探讨不同方法的能力与局限,以及研究人员希望填补的技术空白。 | ||
10月8日 | 本期《自然》技术特写将关注“无细胞蛋白表达”这种系统。它允许研究人员利用粗细胞提取物或混合纯化蛋白来表达特定蛋白。这在生物制造中常有应用,令研究人员能够控制合成环境,例如在合成生物制药时不必在细胞内生产再进行纯化。 |